7月15日,4066金沙(中国)有限公司许敏教授课题组、灵长类转化医学研究院代绍兴副教授研究团队、南方医科大学左大明教授研究团队以及香港大学袁硕峰教授研究团队合作首次发现并合成新型倍半萜衍生物PAC5,通过激活抗病毒新靶标hnRNPA2B1(heterogeneous nuclear ribonucleoprotein A2B1,异质核核糖核蛋白A2B1),抑制体内外乙肝病毒(HBV)和新型冠状病毒(SARS-CoV-2)感染的重要研究成果,以题为“A hnRNPA2B1 agonist effectively inhibits HBV and SARS-CoV-2 Omicronin vivo”(异质核核糖核蛋白A2B1激动剂有效抑制乙肝病毒和新型冠状病毒奥密克戎变种的体内感染)的研究长文在《Protein & Cell》(蛋白与细胞)(中科院双一区Top期刊,影响因子15.328)发表。
病毒性疾病是重大公共卫生问题。乙型肝炎病毒(HBV)已经夺走了数百万人的生命,COVID-19大流行正在造成巨大的经济损失和数百万人死亡。HBV是一种慢性病毒性疾病,其主要挑战是消除HBV共价闭合环状DNA(cccDNA)并减少抗原载量,特别是乙型肝炎表面抗原(HBsAg)。而COVID-19的主要挑战是SARS-CoV-2具有免疫逃避能力和不断出现的遗传变异。疫苗产品是预防HBV和SARS-CoV-2感染的有效手段,但不能用于临床治疗。因此发现具有广谱抗病毒活性的新型化合物和新靶标蛋白对于开发对慢性和急性病毒性疾病的治疗新药尤为重要。
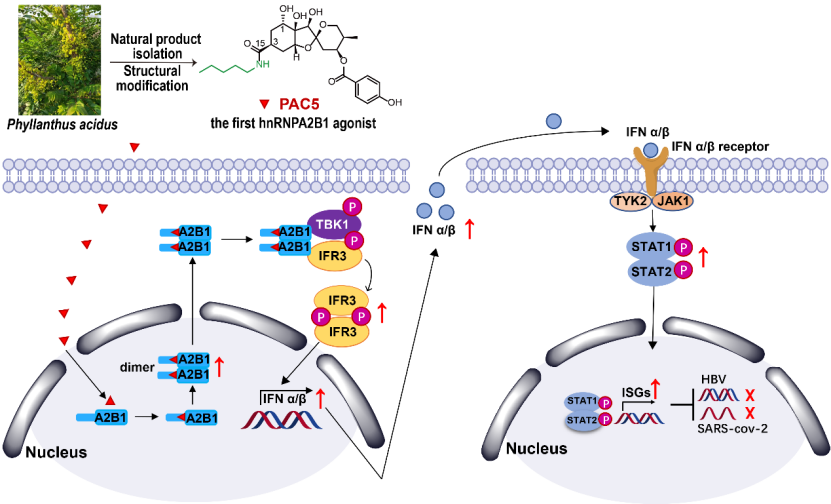
许敏教授课题组基于云南省民族民间药物资源,从抗HBV民族药中发现并通过构效优化获得了天然新型倍半萜衍生物PAC5,可有效治疗HBV和SARS-CoV-2感染,并通过化学生物学手段证明PAC5是新靶标异质核糖核蛋白A2B1(hnRNPA2B1)的首个小分子激动剂。hnRNPA2B1是病原体DNA的核传感器,在抗病毒先天免疫反应中起着至关重要的作用,具有非常重要的生物学功能。研究发现PAC5在HepG2.2.15,HepG2(用PBSK-rtM204I转染),HepAD38细胞和患有HBV感染的原代人肝细胞中均显示显著抑制HBV活性。在HBV感染的两种不同小鼠模型中,PAC5能清除HBV cccDNA并降低HBV相关抗原表达,口服PAC5也显著改善了仓鼠模型中SARS-CoV-2感染引起的肺损伤,并显著抑制了病毒感染。通过设计生物素探针和荧光探针揭示PAC5是hnRNPA2B1的高选择性和强效激动剂,hnRNPA2B1是抗病毒免疫治疗的新的潜在药物靶点。
PAC5有望被开发成为宿主靶向的广谱抗病毒药物(HDAs)。研究团队正在洽谈引入外部资本及合作团队,加快推进PAC5抗病毒1.1类原始创新药的临床转化。
该研究成果由4066金沙、南方医科大学、香港大学和格里菲斯大学等机构合作完成。南方医科大学左大明教授和博士研究生陈宇,香港大学蔡建飘为并列第一作者。4066金沙为第一单位,4066金沙许敏教授为通讯作者,灵长类转化医学研究院代绍兴副教授,南方医科大学左大明教授和香港大学袁硕峰教授为共同通讯作者。研究工作受到国家自然科学基金、云南省科技厅Ronald院士工作站、云南省教育厅天然药物化学生物学创新团队和4066金沙学术青蓝人才项目等项目的资助。
 4066金沙许敏教授研究团队长期致力于西南民族药/中药中药物资源分子的高效发现和识别,组装和构效优化,并以此为探针分子,揭示靶标蛋白及其作用机制。已构建云南省药物资源分子库、探索了抗病毒和干预神经系统疾病新天然分子快速发现新策略、天然片段的智能拆分和双极性分子快速组装新技术、靶标蛋白垂钓新方法等。
4066金沙许敏教授研究团队长期致力于西南民族药/中药中药物资源分子的高效发现和识别,组装和构效优化,并以此为探针分子,揭示靶标蛋白及其作用机制。已构建云南省药物资源分子库、探索了抗病毒和干预神经系统疾病新天然分子快速发现新策略、天然片段的智能拆分和双极性分子快速组装新技术、靶标蛋白垂钓新方法等。
 4066金沙代绍兴研究团队围绕“小分子精准调控蛋白质功能”的这一关键科学问题开展研究,利用化学生物信息学和人工智能等工具,整合疾病的多组学数据,开展疾病的靶点识别和新药物发现。以传统中草药和天然产物为出发点,开发了一系列针对多种疾病(传染疾病、癌症、神经退行性疾病等)和多种靶点的活性化合物预测方法和平台。
4066金沙代绍兴研究团队围绕“小分子精准调控蛋白质功能”的这一关键科学问题开展研究,利用化学生物信息学和人工智能等工具,整合疾病的多组学数据,开展疾病的靶点识别和新药物发现。以传统中草药和天然产物为出发点,开发了一系列针对多种疾病(传染疾病、癌症、神经退行性疾病等)和多种靶点的活性化合物预测方法和平台。
原文链接:https://academic.oup.com/proteincell/advance-article-abstract/doi/10.1093/procel/pwac027/6645057
